Программное обеспечение для управления EU MDRкачествадля разработкидля базы данных ODBC
Добавить в папку «Избранное»
Добавить к сравнению
fo_shop_gate_exact_title
Характеристики
- Функция
- для управления, качества, для разработки, для базы данных ODBC, для безопасности, отслеживания, для системы снабжения, для этикетирования
- Применение
- процесса
- Тип
- централизованное
- Другие характеристики
- по индивидуальному заказу
Описание
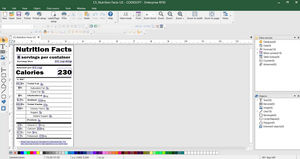
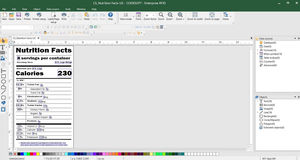
Простое создание и печать этикеток, соответствующих требованиям EU MDR
CODESOFT для создания этикеток, соответствующих стандарту EU MDR
Создание штрихкодов HIBC (Health Industry Barcode) и GS1 Databar
Удобные мастеры
Настройка прав пользователей и контроль безопасности этикеток
Решение TEKLYNX CENTRAL CFR для управления маркировкой
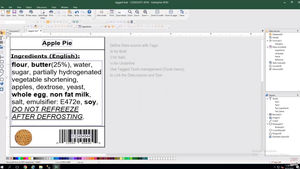
Использование элементов маркировки из централизованной базы данных для создания этикеток, соответствующих требованиям EU MDR
Автоматизация процесса маркировки и централизованное управление гарантируют контроль исполнения процесса и предоставляют дополнительные возможности управления
Организации, распространяющие медицинские устройства на территории ЕС, должны соблюдать требования EU MDR, установленные в мае 2017 года.
Стандарт EU MDR предназначен для охраны здоровья населения и обеспечения безопасности пациентов во всей Европе, а также для повышения качества и прозрачности медицинских изделий в цепочке поставок медицинских компаний посредством стандартизации процессов разработки, утверждения и отслеживания этикеток.
Поэтому на всех этикетках медицинских устройств, за исключением нестандартных устройств и устройств для определения рабочих характеристик, должен быть указан идентификатор Unique Device Identifier (UDI), который включает в себя идентификатор устройства (DI), идентификатор продукта (PI) и информацию в понятном для человека формате (HRI). Начиная с мая 2020 года, производители и дистрибьюторы медицинского оборудования по всей Европе должны будут соблюдать требования к маркировке MDR ЕС.
Каталоги
Для этого товара не доступен ни один каталог.
Посмотреть все каталоги TEKLYNXРасширенный поиск
- Программное обеспечение для автоматизации процесса
- Программное решение для управления
- Программное решение для анализа
- Программное решение процесса
- Программное решение Windows
- Программное обеспечение CAO
- Программное обеспечение для управления
- Программное обеспечение режим реального времени
- Подключенное программное обеспечение
- Программное решение для разработки
- Программное обеспечение для интерфейса
- Программное обеспечение качества
- Автоматизированное программное решение
- Программное решение для сети
- Программное решение развития
- Программное обеспечение для составления отчетности
- Испытательное программное решение
- Программное обеспечение разработки
- Программное обеспечение 2D
- Программное обеспечение для безопасности
* Цены указаны без учета налогов, без стоимости доставки, без учета таможенных пошлин и не включают в себя дополнительные расходы, связанные с установкой или вводом в эксплуатацию. Цены являются ориентировочными и могут меняться в зависимости от страны, цен на сырьевые товары и валютных курсов.